Поражение кирпичной кладки солевыми системами.
Физико-химические основы
- 1. Воздействие солей на кирпич
Капиллярно-пористая структура строительных материалов, обусловленная их природой, структурой и старением, создает известные предпосылки для разрушения.
Причинами природных и техногенных разрушений кирпичной кладки являются:
- Замораживание – размораживание материала в условиях перепада температур;
- Действие грунтовых вод;
- Засоленность сырьевых материалов – глины и песка.
Высокоразвитая сеть капилляров и пор способствует транспорту воды в стенах сооружения за счет физических причин - так называемого капиллярного подъема. Чем меньше диаметр капилляра, тем больше давление воды и выше уровень подсоса.
Глинистые грунты, способствующие высокому уровню залегания грунтовых вод, скопления талых и дождевых вод, отсутствие эффективных дренажных и гидроизоляционных систем создают условия для капиллярного движения грунтовых и атмосферных вод.
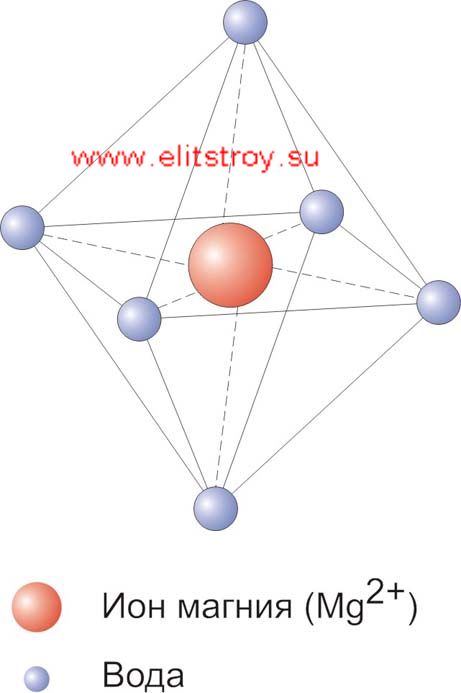
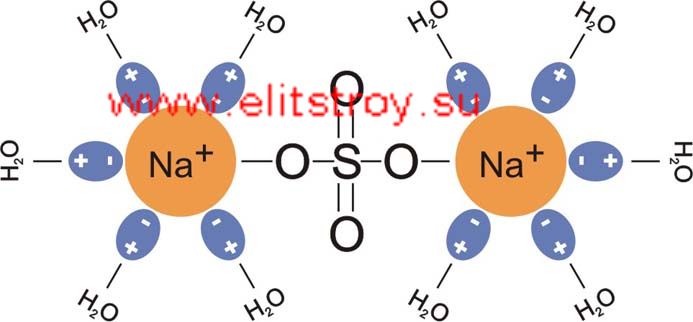
Грунтовые воды представляют собой растворы разнообразных солей. Это гидрокарбонаты кальция и магния, обусловливающие так называемую временную или карбонатную жесткость воды; хлориды и сульфаты щелочных и щелочноземельных металлов – соли постоянной жесткости.
Концентрации солей в природной воде переменны и сильно зависят от специфики региона или местности, интенсивности промышленных и коммунальных сбросов, наличия сельскохозяйственных угодий с массовым применением минеральных удобрений и пр.
Засоленность грунтовых вод, как природного, так и техногенного характера приводит к повышению содержания солей в глиняных и песчаных карьерах. Современный кирпич после обжига не имеет высолов на поверхности, но в условиях атмосферной влажности покрывается разводами солей, где преимущественное место занимают водорастворимые и гигроскопичные сульфаты и хлориды натрия, кальция и магния.
Указанные соли в силу особенностей строения катиона являются агрессивными по отношению к строительным материалам и кирпичу, в частности.
Магний, кальций и натрий имеют малые размеры ионных радиусов – табл. 1, поэтому легко притягивают значительные количества дипольных молекул воды.
Таблица 1.
Радиусы катионов
|
Катион |
Радиус иона, Å |
|
Mg2+ |
0,61 |
|
Са2+ |
1,02 |
|
Na+ |
0,95 |
|
K+ |
1,33 |
Хлориды магния и кальция термодинамически устойчивы в виде кристаллогидратов переменного состава, а сульфат натрия – в виде десятиводного кристаллогидрата Na2SO4.10H2O (табл.2)
Попадая в стены с грунтовыми водами, или растворяясь в кирпиче под действием атмосферной влаги, растворы солей пронизывают капилляры и поры кирпичной массы. В зависимости от температуры и уровня влажности среды в теле кирпича и на его поверхности с той или иной скоростью начинают идти попеременные процессы испарения воды и кристаллизации солей в виде твердых кристаллогидратов – объемных гидрофильных образований.
На рис. 1 представлены: шестиводный сульфат магния, где ион магния образует устойчивый октаэдрический кристаллогидрат, теряющий воду лишь при 200оС, и десятиводный кристаллогидрат сульфата натрия в плоской форме, дегидратирующийся при 32оС.
|
Сульфат магния |
Сульфат натрия |
|
|
|
Рис. 1. Кристаллогидраты солей
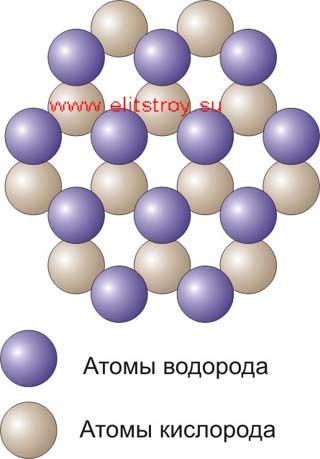
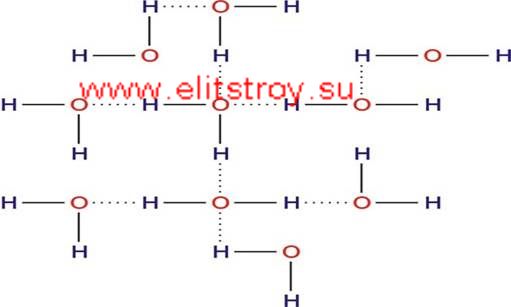
Вода, как известно, имеет полимерную структуру. Ассоциаты полимерных форм в состоянии льда состоят из 5 молекул, а при переходе в жидкую фазу могут включать до 10 и более единичных молекул. Полимерный характер воды обусловлен образованием т.н. водородных связей. Электроотрицательный кислород притягивает протон водорода к свободным электронным парам, и образуется водородная связь, устойчивая до температуры 100оС (рис. 2).
Этим различием в свойствах воды и пара можно объяснить то обстоятельство, что водонепроницаемые системы при соответствующих размерах пор могут быть паропроницаемыми.
|
Лёд |
Вода |
|
|
|
|
|
Рис.2. Полимерная структура воды
По указанным причинам масса и соответственно объем кристаллогидратов на порядок и более могут превышать массу и объём безводной соли.
При насыщении кирпича влагой соли растворяются и затем кристаллизуются повторно при испарении воды. Кроме того, отдельные кристаллогидраты при температурах более 30оС теряют кристаллизационную воду полностью или частично (табл.2), вновь присоединяя ее в вечернее время с уходом солнца и повышением влажности. Эта периодичность наиболее характерна для сульфата натрия, полностью теряющего гидратную воду при температуре 32,4оС, (табл.2).
Таблица 2
Потеря солями кристаллизационной воды
|
MgSO4*7H2O |
150oC |
MgSO4*6H2O |
200oC |
MgSO4*1H2O |
|
Na2SO4*10Н2О |
32,4oC |
Na2SO4 |
|
|
|
Ca(NO3)2*4H2O |
30oC |
Ca(NO3)2*3H2O |
100oC |
Ca(NO3)2 |
|
Na2CO3*10Н2О |
32oC |
Na2CO3*7Н2О |
35,4oC |
Na2CO3*1Н2О |
Возникающее периодически кристаллизационное и гидратационное давление, а также увеличение объема солевой массы неизбежно приводят к деструкции кирпича, табл.3.
Таблица 3
Давление кристаллизации и гидратации солей
|
Соль |
Давление кристаллизации, N/mm2 |
Давление гидратации, N/mm2 |
|
Na2CO3*1Н2О |
28,0 (0оС); 33,3 (50оС) |
|
|
Na2CO3*7Н2О |
10,0 (0OC); 11,9 (50оС) |
93,8 (0оС)*; 61,1 (20оС)* |
|
Na2SO4*10Н2О |
7,2 (0OC); 8,3 (50оС) |
98,2 (0оС)*; 67,4 (20оС)* |
|
Na2SO4 |
29,2 (0оС); 34,5 (50оС) |
|
* - при 100% относительной влажности воздуха
Собственная практика химического анализа солевых соскобов с поверхностей кирпичных фасадов в течение последних 5 лет показала преимущественное присутствие особо опасного для кладки сульфата натрия. Засоленность грунтовых вод и почв (соответственно песка и глины) натриевым сульфатом характерна практически для всех российских регионов, и это можно объяснить не только промышленными, но и в значительной степени - коммунальными стоками, содержащими большие концентрации моющих средств, главным образом, сульфонатов натрия. Органические сульфонаты преобразуются микроорганизмами почв в минеральные сульфаты.
Что касается промышленных вод, то агрессивные стоки в грунты - явление нередкое. Сточные воды коксохимических, металлургических, целлюлозно-бумажных комбинатов чрезвычайно богаты водорастворимыми сульфатами щелочных металлов.
Насыщение почвы сульфатом натрия приводит к сильному солевому загрязнению песка и глины в карьерах. Поэтому новый кирпич уже является источником солей, и белые разводы на его поверхности - не просто эстетический минус, это сигнал опасности, угроза разрушения.
- 2. Как защитить засоленный фасад?
Водорастворимые соли на кладке, кроме указанных выше сульфатов, могут включать еще: хлорид натрия NaCL (поваренная соль), карбонат калия K2CO3 (поташ), карбонат натрия Na2CO3 (сода). Эти соли добавляются в кладочные растворы в период зимней кладки, а затем мигрируют с водой по капиллярной сети материала. Кроме того, цокольные этажи зданий в городах серьезно страдают от солевой нагрузки талых вод (хлористый натрий и хлористый кальций). При намокании в атмосферных условиях и последующем высыхании соли выступают на поверхность под действием капиллярных сил. Удалить их систематической водоструйной обработкой не представляется возможным, ибо процесс выхода солей на поверхность носит перманентный характер – соли стремятся навстречу влаге.
Водонерастворимые соли. Это продукты карбонизации свободной извести, продукты превращения гидрокарбонатов кальция и магния грунтовых вод в карбонаты, а также возможные остатки строительного раствора.
Как очистить кирпич в этом случае?
Ни в коем случае нельзя прибегать к советам случайных людей: например мыть фасад растворами, содержащими соляную кислоту, мазать его соляркой или растительным маслом, покрывать лаками и пр. Все эти «народные» способы наносят кирпичу непоправимый вред. Соляная кислота разрушает кладочный раствор, сильно открывает поры кирпича, и миграция солей на поверхность лишь усиливается, паронепроницаемые лаки начинают шелушиться и отслаиваться под давлением кристаллизующихся солей, а снять их с поверхности фасада часто бывает весьма затруднительно.
Водонерастворимые соли можно удалить без ущерба для поверхности действием разбавленного раствора органической кислоты, например ASO-Steinreiniger (очиститель камня).
Труднее избавиться от растворимых солей, ибо они в форме хлоридов или сульфатов, пронизывают всю кирпичную массу. Оптимальный вариант - перевести соли на поверхности в труднорастворимую форму действием так называемых флюатов – солей кремнефтористоводородной кислоты. Тем самым крупные поверхностные поры окажутся заблокированными для транспорта водорастворимых солей из тела кирпича на поверхность, и перспектива кристаллизационного давления на отделочный слой существенно снижается.
После механической очистки стен от выступивших труднорастворимых образований рекомендуется оштукатуривание фасада пористыми известково-цементными растворами. Цементно-песчаные штукатурки плохо пропускают пар, и это в условиях конденсации приводит к намоканию несущих стен и отслоению покрытий.
Применение гидрофобных, пористых, трещиностойких штукатурок (например, сиcтема THERMOPAL) создает реальную возможность долговечной защиты фасада. Легкая штукатурка (до 30% воздушных гидрофобизованных пор) не принимает на себя функций несущих конструкций и не деформируется при осадке дома. Такие штукатурки обладают способностью «дышать», т.е. пропускать пары воды без конденсации на границе раздела, равномерно распределяют частично мигрирующие соли в порах, не давая им скапливаться в разделительном слое и срывать покрытие. Гидрофобизованные поры защищают штукатурку от внешнего воздействия влаги и воды.
Можно применять порообразующую добавку THERMOPAL-Р, используя в качестве вяжущих – известь и цемент, что тоже сделает штукатурную систему более легкой и паропроницаемой.
Штукатурки THERMOPAL эффективны при защите цокольных частей зданий, подвергающихся серьезной водно-солевой нагрузке в период таяния снега.
Если оставить кирпичный фасад в натуральном виде, без оштукатуривания, следует избавиться от поверхностных солей и предпринять соответствующие защитные меры:
а) очистить фасад разбавленным раствором упомянутого выше кислотного очистителя на базе органической кислоты, который удалит остатки строительного раствора, растворимые и труднорастворимые соли и освободит поры поверхности;
б) пропитать фасад гидрофобизирующей жидкостью. Как правило, это кремнийорганические композиции в виде растворов или водных дисперсий. Активная часть композиции отверждается в атмосферных условиях, выстилая стенки капилляров и пор защитной водонепроницаемой, но паропроницаемой пленкой. Чем меньше воды в составе пропиточного раствора, тем быстрее идет процесс отверждения. Наиболее эффективными гидрофобизаторами являются кремнийорганические жидкости силоксанового типа на органических растворителях (ASOLIN-WS). В результате гидрофобизации капли воды скатываются с фасада, не впитываясь в материал и не давая глубинным солям возможности выхода на поверхность.
Солевые нагрузки на кирпич – факт повсеместный. И с этим следует серьёзно считаться, продумывая еще на стадии проекта комплекс защитных гидроизоляционных и гидрофобизационных мер.